Употребление алкоголя давно известно как один из ведущих факторов риска заболеваний печени, включая жировую дистрофию, гепатит и цирроз. Однако до недавнего времени оставалось не до конца понятным, какие именно молекулярные механизмы связывают поступление этанола в организм с массовой гибелью клеток печени и развитием воспаления. Особенно актуальным этот вопрос становится в свете данных о том, что вирусные инфекции (например, гепатит В, гепатит С или COVID-19) значительно усиливают повреждающее действие алкоголя. Исследование, опубликованное в журнале Science Advances (том 12, номер 15, статья eaea3979), раскрывает этот механизм на уровне работы врожденной иммунной системы. Авторами работы выступили исследователи под руководством Rajendra Karki (Стоматологический факультет Сеульского национального университета, Республика Корея) и SangJoon Lee (Ульсанский национальный институт науки и технологий, Республика Корея), а также Si Ming Man (Австралийский национальный университет, Канберра, Австралия).
Ключевую роль в обнаруженном процессе играет белок ZBP1 (Z-DNA binding protein 1). Этот белок относится к группе так называемых паттерн-распознающих рецепторов — молекул, которые распознают опасные сигналы внутри клетки. В норме ZBP1 участвует в защите от вирусов, но, как выяснили авторы работы, он же может становиться центральным звеном в цепи событий, ведущих к гибели клеток под действием алкоголя. Исследователи показали, что сам по себе этанол не вызывает сильной активации ZBP1. Однако в присутствии интерферонов — сигнальных белков, которые выделяются клетками при вирусных инфекциях или хроническом воспалении, — ситуация резко меняется.
Интерфероны повышают количество белка ZBP1 внутри клетки. Одновременно с этим алкоголь подавляет выработку другого защитного белка — ADAR1 (аденозиндезаминазы, действующей на РНК). В норме ADAR1 выполняет роль «молекулярного тормоза»: он редактирует двуспиральные участки РНК, не давая иммунной системе ошибочно атаковать собственные молекулы организма. Когда уровень ADAR1 падает, а количество ZBP1 растёт, создаются условия для ложного распознавания. Клетка начинает воспринимать собственные молекулы РНК как чужеродные, особенно те из них, которые способны формировать особую Z-конформацию (так называемую Z-РНК).
Важным звеном в этом процессе является сигнальный путь JNK (c-Jun N-терминальная киназа). И алкоголь, и интерфероны по отдельности слабо активируют этот путь, но их совместное действие приводит к мощной и устойчивой активации JNK. Именно JNK-киназа способствует накоплению Z-РНК в цитоплазме клетки. Когда ZBP1 связывается с этой Z-РНК, запускается каскад реакций, который приводит к гибели клетки. Причём гибель эта происходит не по одному, а сразу по трём типам: пироптозу, апоптозу и некроптозу. Все они относятся к воспалительным формам клеточной смерти, то есть сопровождаются выбросом провоспалительных молекул, которые привлекают иммунные клетки и усиливают повреждение тканей.
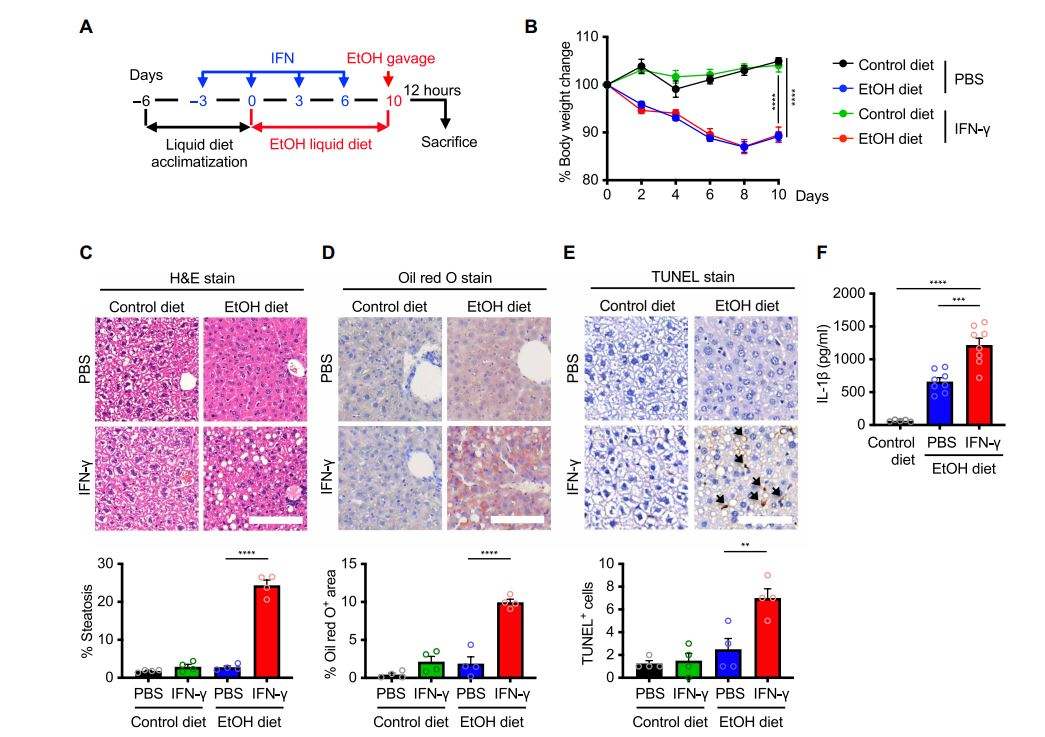
Эксперименты на мышах подтвердили клиническую значимость этого механизма. Животным в течение 10 дней давали алкогольный корм, а затем однократную высокую дозу этанола, что моделирует остро-хроническое поражение печени у человека. Часть мышей дополнительно получала инъекции интерферона-гамма. У животных, получавших и алкоголь, и интерферон, развивались тяжёлые повреждения печени: баллонирование гепатоцитов, жировая дистрофия, появление телец Маллори (признак повреждения цитоскелета), а также инфильтрация воспалительных клеток. У мышей с отключённым геном Zbp1, напротив, поражение печени было значительно слабее, а уровень фермента АЛТ (маркёра гибели клеток печени) в крови — ниже.
Анализ тканей пациентов с алкогольной болезнью печени показал, что у них значительно повышена активность генов, связанных с интерфероновым ответом и работой ZBP1. Также у таких пациентов обнаруживались признаки одновременной активации апоптоза, пироптоза и некроптоза. У здоровых людей или пациентов с неалкогольной жировой болезнью печени этих изменений не наблюдалось. Это говорит о том, что обнаруженный механизм специфичен именно для алкогольного поражения печени, особенно в тех случаях, когда оно сочетается с воспалением или инфекцией.
Полученные результаты имеют важное практическое значение. Во-первых, они объясняют, почему хроническое употребление алкоголя особенно опасно на фоне вирусных инфекций. Во-вторых, они открывают новые мишени для лекарственной терапии. Теоретически, блокирование белка ZBP1, подавление пути JNK или восстановление уровня ADAR1 могут предотвратить гибель клеток и развитие тяжёлых форм алкогольной болезни печени. Авторы работы подчёркивают, что, поскольку в процесс вовлечено сразу несколько типов клеточной смерти, воздействовать необходимо на верхние звенья цепи — на сам сенсор ZBP1 или на образование Z-РНК, а не на отдельные эффекторные молекулы. Это может стать основой для разработки принципиально новых подходов к лечению алкоголь-ассоциированных заболеваний печени.